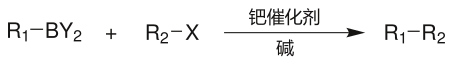鈴木反應
鈴木反應(日語:鈴木反応,英語:Suzuki reaction),也稱作鈴木偶聯反應(日語:鈴木カップリング、英語:Suzuki coupling)、鈴木-宮浦反應(日語:鈴木・宮浦反応,英語:Suzuki-Miyaura reaction),是一個有機偶聯反應,是在鈀配合物催化下,芳基或烯基的硼酸或硼酸酯與氯、溴、碘代芳烴或烯烴發生交叉偶聯。[1][2]
| 鈴木反應 | |
|---|---|
| 命名根據 | 鈴木章 |
| 反應類型 | 偶聯反應 |
| 標識 | |
| 有機化學網站對應網頁 | 鈴木偶聯 |
| RSC序號 | RXNO:0000140 |
該反應由鈴木章(日語:鈴木 章/すずき あきら Suzuki Akira)在1979年首先報道,在有機合成中的用途很廣,具有很強的底物適應性及官能團耐受性,常用於合成多烯烴、苯乙烯和聯苯的衍生物,從而應用於眾多天然產物、有機材料的合成中[3][4][5]。鈴木章也憑藉此貢獻與理查德·赫克、根岸英一共同獲得2010年諾貝爾化學獎[6]。
2018年,鈴木反應被成功地轉移到異相體系中進行。[7]
概述
編輯鈴木反應對官能團的耐受性非常好,反應物可以帶着-CHO、-COCH3、-COOC2H5、-OCH3、-CN、-NO2、-F等官能團進行反應而不受影響。反應有選擇性,不同鹵素、以及不同位置的相同鹵素進行反應的活性可能有差別,三氟甲磺酸酯、重氮鹽、碘鎓鹽或芳基鋶鹽和芳基硼酸也可以進行反應,活性順序如下:
另一個廣泛應用的底物是芳基硼酸,由芳基鋰或格氏試劑與烷基硼酸酯反應製備(見宮浦硼酸化反應,宮浦反應)。這些化合物對空氣和水蒸氣比較穩定,容易儲存。鈴木反應靠一個四配位的鈀催化劑催化,廣泛使用的催化劑為Pd(PPh3)4(0)與PdCl2(dppf),其他的配體還有:AsPh3、n-Bu3P、(MeO)3P,以及雙齒配體Ph2P(CH2)2PPh2(dppe)、Ph2P(CH2)3PPh2(dppp)等。 (以上的所有Pd配體都是厭氧的,因此反應必須在氮氣,氬氣等惰性氣體下反應)。[8]
鈴木反應中的鹼也有很多選擇,最常用的是碳酸鈉、碳酸銫、醋酸鉀、磷酸鉀等。 鹼金屬碳酸鹽中,活性順序為:
而且,加入氟離子(F−)會與芳基硼酸形成氟硼酸鹽負離子,可以促進硼酸鹽中間體與鈀中心的反應。 因此,氟化四丁基銨、氟化銫、氟化鉀等化合物都會使反應速率加快,甚至可以代替反應中使用的鹼。
機理
編輯反應機理見下圖。首先鹵代烴2與零價鈀進行氧化加成,與鹼作用生成強親電性的有機鈀中間體4[9]。同時芳基硼酸與鹼作用生成酸根型配合物四價硼酸鹽中間體6,具親核性,與4作用生成8。最後8經還原消除,得到目標產物9以及催化劑1。
氧化加成一步,用乙烯基鹵反應時生成構型保持的產物,但用烯丙基和苄基鹵反應則生成構型翻轉的產物[10]。這一步首先生成的是順式的鈀配合物,而後立即轉變為反式的異構體。[11]
還原消除得到的是構型保持的產物[12]。
討論
編輯對於一些SP3雜化的烷基硼或者硼酸化合物,同樣可以發生反應稱為硼-烷基鈴木-宮浦交叉耦聯反應。 與鈴木偶聯相比它有若干缺點:1.反應進程慢;2.自身耦聯副產物較多;3.和磷配體耦聯的副產物多;4.可能會造成手性消旋或者羥醛縮和反應。[13][14][15][16][17]
展望
編輯鈴木-宮浦交叉耦聯在有機合成當中的最新應用已經被Kotha和同事歸納。[18]當SPhos(一種有機膦配體)參與反應,其催化劑的用量聲稱可以降低至0.001 mol%。[19]
參見
編輯參考文獻
編輯- ^ Miyaura, N. et al. Tetrahedron Lett. 1979, 3437.
- ^ Miyaura, N.; Suzuki, A. Chem. Commun. 1979, 866.
- ^ 反應綜述參見:Suzuki, A. Pure Appl. Chem. 1991, 63, 419-422. (Review)
- ^ Miyaura, N.; Suzuki, A. Chem. Rev. 1995, 95, 2457-2483. doi:10.1021/cr00039a007
- ^ Suzuki, A. J. Organometallic Chem. 1999, 576, 147–168.
- ^ Akira Suzuki - Biographical. Nobelprize.org. 2010-10-06 [2011-02-23]. (原始內容存檔於2011-05-12).
- ^ Chen, Zupeng; Vorobyeva, Evgeniya; Mitchell, Sharon; Fako, Edvin; Ortuño, Manuel A.; López, Núria; Collins, Sean M.; Midgley, Paul A.; Richard, Sylvia; Vilé, Gianvito; Pérez-Ramírez, Javier. A heterogeneous single-atom palladium catalyst surpassing homogeneous systems for Suzuki coupling. Nature Nanotechnology. 2018-08, 13 (8): 702–707. doi:10.1038/s41565-018-0167-2.
- ^ 邢其毅等。《基礎有機化學》第三版下冊.北京:高等教育出版社,2005年.ISBN 978-7-04-017755-8.
- ^ Matos, Karl; Soderquist, John A. Alkylboranes in the Suzuki−Miyaura Coupling: Stereochemical and Mechanistic Studies. The Journal of Organic Chemistry. 1998-02, 63 (3): 461–470. doi:10.1021/jo971681s.
- ^ Stille, John K.; Lau, Kreisler S. Y. Mechanisms of oxidative addition of organic halides to Group 8 transition-metal complexes. Accounts of Chemical Research. 1977-12-01, 10 (12): 434–442. doi:10.1021/ar50120a002.
- ^ Casado, A. L.; Espinet, P. Organometallics 1998, 17, 954–959.
- ^ Ridgway, Brian H.; Woerpel, K. A. Transmetalation of Alkylboranes to Palladium in the Suzuki Coupling Reaction Proceeds with Retention of Stereochemistry. The Journal of Organic Chemistry. 1998-02, 63 (3): 458–460. doi:10.1021/jo970803d.
- ^ Littke, A. F., Fu, G. C. A convenient and general method for Pd-catalyzed Suzuki cross-couplings of aryl chlorides and arylboronic acids. Angew. Chem., Int. Ed. Engl. 1999, 37, 3387-3388.
- ^ Wolfe, J. P., Singer, R. A., Yang, B. H., Buchwald, S. L. Highly Active Palladium Catalysts for Suzuki Coupling Reactions. J. Am. Chem. Soc. 1999, 121, 9550-9561.
- ^ Netherton, M. R., Dai, C., Neuschuetz, K., Fu, G. C. Room-Temperature Alkyl-Alkyl Suzuki Cross-Coupling of Alkyl Bromides that Possess β Hydrogens. J. Am. Chem. Soc. 2001, 123, 10099-10100.
- ^ Kirchhoff, J. H., Dai, C., Fu, G. C. A method for palladium-catalyzed cross-couplings of simple alkyl chlorides: Suzuki reactions catalyzed by [Pd2(dba)3]/PCy3. Angew. Chem., Int. Ed. Engl. 2002, 41, 1945-1947.
- ^ Molander, G. A., Bernardi, C. R. Suzuki-Miyaura Cross-Coupling Reactions of Potassium Alkenyltrifluoroborates. J. Org. Chem. 2002, 67, 8424-8429.
- ^ Recent applications of the Suzuki–Miyaura cross-coupling reaction in organic synthesis Sambasivarao Kotha, Kakali Lahiri and Dhurke Kashinath Tetrahedron 2002, 48, 9633-9695 doi:10.1016/S0040-4020(02)01188-2
- ^ Catalysts for Suzuki-Miyaura Coupling Processes: Scope and Studies of the Effect of Ligand Structure Timothy E. Barder, Shawn D. Walker, Joseph R. Martinelli, and Stephen L. Buchwald J. AM. CHEM. SOC. 2005, 127, 4685-4696 doi:10.1021/ja042491j