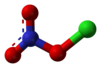
硝酸氯
化合物
硝酸氯是存在于大气平流层中一种重要气体,化学式为ClNO3。它是导致臭氧消耗的重要氯源。
| 硝酸氯 | |||
|---|---|---|---|
| |||

| |||
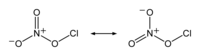
| |||
| IUPAC名 Chlorine nitrate | |||
| 系统名 Chloro nitrate | |||
| 别名 | 次氯酸硝酰酯 | ||
| 识别 | |||
| CAS号 | 14545-72-3 | ||
| PubChem | 114934 | ||
| ChemSpider | 102875 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | XYLGPCWDPLOBGP-UHFFFAOYSA-N | ||
| 性质 | |||
| 化学式 | ClNO3 | ||
| 摩尔质量 | 97.46 g·mol⁻¹ | ||
| 密度 | 1.65 g/cm3 | ||
| 熔点 | −101 °C(172 K) | ||
| 危险性 | |||
GHS危险性符号 
| |||
| GHS提示词 | Danger | ||
| NFPA 704 | |||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
化学性质
编辑硝酸氯与金属、金属氯化物、醇、醚和多数有机化合物发生剧烈反应并可能爆炸。受热分解会放出有毒的Cl2和NOx。
制备和反应
编辑硝酸氯的制备方法是在0 °C下由一氧化二氯与五氧化二氮反应:[1]
- Cl2O + N2O5 → 2 ClONO2
- ClF + HNO3 → HF + ClONO2
它还可以与烯烃发生反应:
- (CH3)2C=CH2 + ClONO2 → O2NOC(CH3)2CH2Cl
- 4 ClONO2 + TiCl4 → Ti(NO3)4 + 4 Cl2
参考资料
编辑- ^ Schmeisser, M.; Ruff, J. K. & Lustig, M. Chlorine(1) Nitrate Inorganic Syntheses, Wiley-Blackwell, https://doi.org/10.1002/9780470132401.ch34, 1967, 127-130
- ^ Schack, Carl J. New synthesis of chlorine nitrate. Inorganic Chemistry. 1967-10-01, 6 (10): 1938–1939. ISSN 0020-1669. doi:10.1021/ic50056a047.
- ^ 张青莲. 《无机化学丛书》第六卷:卤素、铜分族、锌分族. 北京: 科学出版社. 1991: P338–341. ISBN 7-03-002238-6.