硫脲
硫脲是尿素中的氧被硫替代后形成的化合物,属于硫代酰胺(RC(S)NR2,R为烃基)。由于电负性差异,尽管结构类似,硫脲和尿素的性质很不相同。硫脲在有机合成中有广泛应用。
| 硫脲 | |
|---|---|

| |
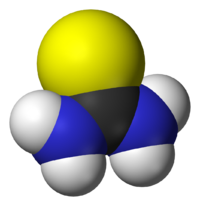
| |
| IUPAC名 Thiourea | |
| 识别 | |
| CAS号 | 62-56-6 |
| PubChem | 2723790 |
| ChemSpider | 2005981 |
| SMILES |
|
| InChI |
|
| InChIKey | UMGDCJDMYOKAJW-UHFFFAOYAJ |
| Beilstein | 605327 |
| Gmelin | 1604 |
| UN编号 | 2811 |
| ChEBI | 36946 |
| RTECS | YU2800000 |
| KEGG | C14415 |
| 性质 | |
| 化学式 | CH4N2S |
| 摩尔质量 | 76.1219 g·mol⁻¹ |
| 密度 | 1.405 g/ml |
| 熔点 | 176-178°C |
| 溶解性(水) | 95, 10 °C 137, 20 °C |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
结构
编辑硫脲是平面分子。在各种硫脲衍生物中 C=S 键长并没有很大差别,均在1.60±0.1Å范围内。C-N键在某种程度上有双键性质,因此硫脲和尿素类似,不易发生反应。
硫脲具有互变异构。在水溶液中,以下平衡偏向左边:
合成
编辑世界上每年硫脲的产量大约有10000吨,其中大约40%是在中国,40%在德国,20%在日本。硫脲可由硫氰酸铵制取,但主要还是由二氧化碳存在下氨氰化钙和硫化氢反应得到。
比较重要的N,N-取代的硫脲可以通过乙醚作溶剂,由相应的氨腈与LiAlHSH在盐酸存在下合成。而LiAlHSH可由硫和氢化铝锂反应得到。
应用
编辑硫脲可以还原过氧化物为相应的二醇。例如在下面的反应中,环戊二烯首先与单线态氧环加成为一个不稳定的环过氧化物中间体,然后用硫脲还原,便得到相应的二醇。
因此硫脲也被用于烯烃的臭氧化,即还原中间体臭氧化物为相应羰基化合物。甲硫醚也可以进行类似反应,但由于它的易挥发性和难闻的气味使得其应用受限。而硫脲难挥发,且没有气味,因此应用较多。
硫脲还被用于将卤代烃转化为硫醇,中间产物是异硫脲盐。反应机理是:
这个反应显示出含硫中心的强亲核性,及异硫脲盐的易水解性。碱金属硫化物也可进行该反应,但会产生二烷基硫醚。硫脲的使用避免了副产物的生成。
硫脲也可用于嘧啶环系的构建,具体过程是:硫脲中的氨基与β-二羰基化合物中的羰基及烯醇缩合,然后脱硫。
硫酸镉和硫脲反应可以制得半导体硫化镉纳米粒子。具体过程是:含有1g硫酸镉(1.3mmol),0.5g硫脲(6.6mmol)和0.1g二氧化硅的浊液在超声波存在下通风室温反应3小时。反应物颜色变黄则表明了产物硫化镉的生成。
硫脲被用于阻燃树脂、橡胶硫化促进剂、晒图纸(感光复印纸)及几乎所有复印纸的生产。硫脲法提金、银避免了用传统氰化法产生的氰化物的污染和气味。
危险
编辑参考资料
编辑- C. Kaneko, A. Sugimoro, and S. Tanaka. A facile one-step synthesis of cis-2-cyclopentene and cis-2-cyclohexene-1,4-diols from the corresponding cyclodienes. “Synthesis”. 876, (1974).
- Gupta, D., Soman, G., and Dev, S.. Thiourea, a convenient reagent for the reductive cleavage of olefin ozonolysis products. “Tetrahedron”. 38, 3013 (1982)
- Speziale, A. J. (1963). "Ethanedithiol (页面存档备份,存于互联网档案馆)". Org. Synth.; Coll. Vol. 4: 401.
- Foster, H. M., and Snyder, H. R. (1963). "4-Methyl-6-hydroxypyrimidine (页面存档备份,存于互联网档案馆)". Org. Synth.; Coll. Vol. 4: 638.
- Dodson, R. M., and King, L. C.. The reaction of ketones with halogens and thiourea. “J. Am. Chem. Soc.”, 67, 2242 (1945).
- The Chemistry of double-bonded functional groups edited by S. Patai. pp 1355-1496. John Wiley & Sons. New York, NY, 1977. ISBN 0-471-92493-8.