拉氏图
拉氏图(又名 Ramachandran 图、[φ,ψ]图、α-碳与酰胺平面交角图,英語:Ramachandran plot, Rama plot),起初是于1963年由 G. N. Ramachandran,C. Ramakrishnan 和 V. Sasisekharan 提出的[1],是一种使蛋白质结构中,主链氨基酸残基的二面角 ψ 和 φ 可视化的方法。
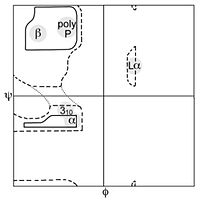
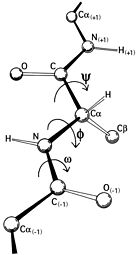
左侧的图形说明了主链二面角φ 和 ψ 的定义(当时被Ramachandran叫做 φ 和 φ')[2]。肽键处的 ω 角通常是 180°,因为肽键的部分双键性质使它保持平面结构[3]。右上方的图,则展示了由 Ramachandran 等人于 1963年 至 1968年根据刚性球面模型计算得到的主链 φ,ψ 二面角允许的构象区域:完全允许的以实线表示,部分允许的则是虚线,点线则表示松弛的τ(N-Cα-C)角[4]。由于二面角的值 0° 和 360° 是等效的,拉氏图的边缘可以从左到右和从上到下“卷”起来。比如说,左下角的允许区的小条就可以与左上方的大的构象允许区域连接起来。
应用
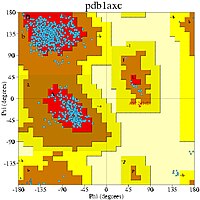
编辑拉氏图可以用于多少有些不同的两种方面。一个从理论上展示哪些 ψ 和 φ 二面角的组合(或者说构象)对于蛋白质中的氨基酸残基(如右上图)是有可能的。其二是展示观测数据点的经验分布(如右图),用于结构确认中,或者在许多结构所组成的数据库中(如左下3幅图所示)。这两种情况均常用于展示理论偏好区域的外形。
氨基酸偏好
编辑可以预料,更大的侧链将会导致其更受限制,从而表现在拉氏图上是一个更小的允许区域。实际上看起来并不是这样;只有β-位碳原子处的亚甲基的影响比较大。甘氨酸的侧链只是一个氢原子,比起所有其它氨基酸侧链开头的 -CH3, -CH2-, 或-CH< 有一个更小的范德华半径,所以它是受限制最小的,这在甘氨酸的拉氏图中(见左图,甘氨酸)可以看出,其允许区域大多了。相反,脯氨酸的拉氏图,由于其侧链与主链 α-C 及 N 形成五元环,则表现出 ψ 和 φ 的非常有限的可能组合(见左图,脯氨酸)
近期的更新
编辑第一个拉氏图于原子水平的蛋白质结构(肌红蛋白,1960)首次测定后被计算出来,虽然其结论是基于短肽的小分子晶体学上。如今,几十年过去了,已经有几万种通过X-射线晶体学测定并存储于蛋白质资料库(PDB)的蛋白质的高分辨率结构。很多研究已经利用了这个数据以产生更加详细精确的φ,ψ图(Morris et al. 1992;[5] Kleywegt & Jones 1996;[6] Hooft et al. 1997;[7] Hovmöller et al. 2002;[8] Lovell et al. 2003[9])。左侧的三个图展示了来自一系列高解析度的结构的数据点以及通常情况(除甘氨酸,脯氨酸及 pre-Pro之外所有氨基酸),甘氨酸及脯氨酸的偏好和允许的构象区域的轮廓。最常见的区域标记如下:α 表示 α-螺旋,Lα 表示左旋α-螺旋,β 表示 β-折叠,ppII表示聚脯氨酸II。
相关
编辑也可以对多糖以及其它聚合物中的二面角类似作图(例如,通过CARP等)。对蛋白质的前两个侧链二面角有一个相似的图:Janin图。
图库
编辑-
通常情况下的拉氏图; 数据来自 Lovell, 2003
-
甘氨酸的拉氏图
-
脯氨酸的拉氏图
-
pre-Proline的拉氏图
相关软件
编辑- 拉氏图 2.0
- Web-based tool showing Ramachandran plot of any PDB entry
- MolProbity web service that produces Ramachandran plots and other validation of any PDB-format file (页面存档备份,存于互联网档案馆)
- STING
- PyMOL,具有 DynoPlot 扩展。
- VMD, distributed with dynamic Ramachandran plot plugin
- WHAT_CHECK,来自WHAT_IF_software的独立验证的程序。
- UCSF Chimera,可以在 Model Panel 中找到。
- Sirius可视化软件
- Swiss PDB Viewer (页面存档备份,存于互联网档案馆)
- TALOS (页面存档备份,存于互联网档案馆)
参见蛋白质资料库条目,其中列出了更多类似的软件。
参考来源
编辑- ^ Ramachandran, G.N.; Ramakrishnan, C.; Sasisekharan, V. Stereochemistry of polypeptide chain configurations. Journal of Molecular Biology. 1963, 7: 95–9. PMID 13990617. doi:10.1016/S0022-2836(63)80023-6.
- ^ Richardson, J.S. Anatomy and Taxonomy of Protein Structures. Advances in Protein Chemistry. Advances in Protein Chemistry. 1981, 34: 167–339. ISBN 9780120342341. PMID 7020376. doi:10.1016/S0065-3233(08)60520-3.
- ^ Pauling, L.; Corey, H.R.; Branson, H. R. The Structure of Proteins: Two Hydrogen-Bonded Helical Configurations of the Polypeptide Chain. Proceedings of the National Academy of Sciences of the United States of America. 1951, 37 (4): 205–211. PMC 1063337 . PMID 14816373. doi:10.1073/pnas.37.4.205.
- ^ Ramachandran, G.N.; Sasiskharan, V. Conformation of polypeptides and proteins. Advances in Protein Chemistry. Advances in Protein Chemistry. 1968, 23: 283–437. ISBN 9780120342235. PMID 4882249. doi:10.1016/S0065-3233(08)60402-7.
- ^ Morris, A.L.; MacArthur, M.W.; Hutchinson, E G.; Thornton, J.M. Stereochemical quality of protein structure coordinates. Proteins: Structure, Function, and Genetics. 1992, 12 (4): 345–64. PMID 1579569. doi:10.1002/prot.340120407.
- ^ Kleywegt, G.J.; Jones, T.A. Phi/psi-chology: Ramachandran revisited. Structure. 1996, 4 (12): 1395–400. PMID 8994966. doi:10.1016/S0969-2126(96)00147-5.
- ^ Hooft, R.W.W.; Sander, C.; Vriend, G. Objectively judging the quality of a protein structure from a Ramachandran plot. Comput Appl Biosci. 1997, 13 (4): 425–430. doi:10.1093/bioinformatics/13.4.425.
- ^ Hovmöller, S.; Zhou, T.; Ohlson, T. Conformations of amino acids in proteins. Acta Crystallographica D. 2002, 58 (Pt 5): 768–76 [2011-11-01]. PMID 11976487. doi:10.1107/S0907444902003359. (原始内容存档于2018-06-04).
- ^ Lovell, S.C.; Davis, I.W.; Arendall, W.B.; De Bakker, P.I.W.; Word, J.M.; Prisant, M.G.; Richardson, J.S.; Richardson, D.C. Structure validation by Cα geometry: ϕ,ψ and Cβ deviation. Proteins: Structure, Function, and Genetics. 2003, 50 (3): 437–50. PMID 12557186. doi:10.1002/prot.10286.
更多阅读
编辑- 张楚富. 生物化学原理. ISBN 978-7-04-029978-6 (中文(简体)).